2018一级结构工程师基础普通化学练习题(3)
1.定性比较下列四种溶液(浓度都是0.1 molkg-1)的沸点,沸点高的是( )
A.Al3(SO4)3 B.MgSO4 C.CaCl2 D.CH3CH3OH
2. 根据酸碱质子理论,下列化学物质中既可作为酸又可以作为碱的是 答( )
A.NH4+ B.HCO3- C.H3O+ D.NaAc
3.25oC度时, Ka(HCN)=4.9×10-10,则0.010mol.dm-3 HCN水溶液中的C(H+)为( )
A .2.2×10-6mol .dm -3 B. 4.9×10-12mol .dm -3
C .1.0×10-4mol .dm -3 D.2.2×10-5mol .dm -3
|
试题来源:[2018一级注册结构工程师考试焚题库] 查看试题答案,请扫描二维码,立即获得本题库手机版 咨询电话:4000-525-585! |
|
4.在0.05moldm-3的HCN中,若有0.010/0的HCN电离了,则HCN的解离常数Ka为( )
A.5×10-8 B.5×10-10 C.5×10-6 D.2.5×10-7
5.已知某一元弱酸的浓度为0.01mol.dm-3,pH=4.55,则其解离常数Ka为( )
A.5.8×10-2 B.9.8×10-3 C.8.6×10-7 D.7.97×10-8
6.在氨水中加入一些NH4Cl晶体,会使( )
A、NH3水的解离常数增大 B、NH3水的解离度a增大
C、溶液的pH值增大 D、溶液的pH值降低
7. NaHCO3-Na2CO3组成的缓冲溶液pH值为 ( )
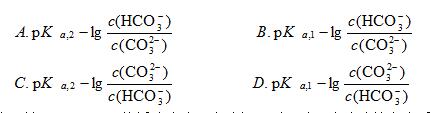
8.欲配制500mLpH=5.0的缓冲溶液,应选择下列哪种混合溶液较为合适( )A.HAc-NaAc(Ka=1.75×10-5)
B.NH3・H2O-NH4Cl(Kb=1.74×10-5)
C.NaH2PO4-Na2HPO4(Ka2=6.31×10-8)
D.NaHCO3-Na2CO3(Ka2=4.68×10-11)
9.在某温度时,下列体系属于缓冲溶液的是( )
A. 0.100 mol.dm-3的NH4Cl溶液;
B. 0.100 mol.dm-3的NaAc溶液;
C. 0.400 mol.dm-3的HCl与0.2 00mol.dm-3NH3.H2O等体积混合的溶液;
D. 0.400 mol.dm-3的NH3.H2O与0.2 00mol.dm-3HCl等体积混合的溶液.
10.在100ml的0.14mo1. dm-3HAc溶液中, 加入100ml的0.10mol. dm-3NaAc溶液, 则该溶液的PH值是(计算误差+-0.01PH单位) ( )
A.9.40 B.4.75 C.4.60 D.9.25
注:HAc的Pka=4.75
- ・2019年一级结构工程师《全科》考试题库我要购买
- ・2019年一级结构工程师《基础考试》考试题库我要购买
- ・2019年二级结构工程师《专业考试》考试题库我要购买
- ・2019年一级结构工程师《专业考试》考试题库我要购买
- 12019-08-022019一级注册结构工程师《土木工程施工与管理》考点冲刺汇总
- 22019-08-022019年广西一级结构工程师基础考试科目
- 32019-08-02专科学历能报考广西二级结构工程师考试吗?
编辑推荐
- 考试题库
- 模拟试题
- 历年真题


