1.在容量瓶上无需有标记的是
A.标线 B.温度 C.浓度 D.容量
2.某实验需要0.2 mol NaOH固体,用托盘天平称取固体时,天平读数(游码及砝码)将
A.等于8.0g B.等于8.00g
C.大于8.0g D.等于0.2g
3.0.5L 1mol/L的FeCl3溶液与0.2L 1 mol/L的KCl溶液中,Cl-浓度比为
A.15∶2 B.1∶1 C.3∶1 D.1∶3
4.相对分子质量为M的某物质在室温下的溶解度为S g,此时测得饱和溶液的密度为ρg・cm-3,则该饱和溶液的物质的量浓度是

5.将标准状况下的a L HCl(气)溶于1000g水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度是
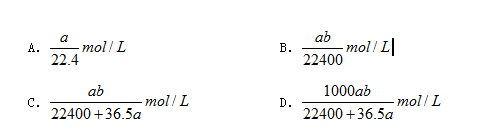
6.NA为阿伏加德罗常数,下列关于0.2mol/L K2SO4溶液的正确说法是
A.500mL溶液中所含K+、SO42-总数为0.3NA
B.500mL溶液中含有0.1NA个K+离子
C.1L溶液中K+离子浓度是0.2mol/L
D.2L溶液中SO42-离子浓度是0.4mol/L
7.取100mL 0.3mol/L和300mL 0.25mol/L的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是
A.0.21mol/L B.0.42mol/L
C.0.56mol/L D.0.26mol/L
8.某Al2(SO4)3溶液V mL中含a g Al3+,取出V/4 mL溶液稀释成4V mL后,SO42-的物质的量浓度为
A.125/54V mol・L-1 B.125a/36V mol・L-1
C.125a/18V mol・L-1 D.125a/V mol・L-1
9.将2.4mol某金属投入1.8L 2mol/L的某酸溶液中,恰好完全反应,并产生7.2g氢气,则该金属和酸分别是
A.二价金属,二元酸
B.二价金属,三元酸
C.三价金属,二元酸
D.一价金属,一元酸
10.配制一定体积、一定物质的量浓度的溶液,实验结果产生偏低影响的是
A.容量瓶中原有少量蒸馏水
B.溶解所用的烧杯未洗涤
C.定容时仰视观察液面
D.定容时俯视观察液面
11.有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,则此溶液中K+的物质的量浓度为
A.0.1mol/L B.0.15mol/L
C.0.2mol/L D.0.25mol/L
12.在100g浓度为18mol/L、密度为ρ的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加入水的体积
A.小于100mL B.等于100mL
C.大于100mL D.等于100/P.ML
13.用密度为1.32g/cm3的硫酸溶液逐滴滴入到BaCl2溶液中,直到沉淀恰好完全为止。已知所生成的溶液的质量等于原BaCl2溶液的质量,则H2SO4溶液的浓度为
A.21.9% B.42.1%
C.13.5mol/L D.5.67mol/L
14.质量为8.02g的铁片,放进1.0L 0.90mol/L的CuSO4溶液中,过一段时间取出洗净、干燥、称量,质量为8.66g。若认为溶液的体积没有变化,则Cu2+的浓度变为
A.0.89mol/L B.0.82mol/L
C.0.78mol/L D.0.6mol/L
15.将4gNaOH溶解在10mL水中,稀至1L后取出10mL,其物质的量浓度是
A. 1mol/L B. 0.1mol/L
C. 0.01mol/L D. 10mol/L